
诱导多能干细胞(iPSC)的发现源于2006年京都大学山中伸弥教授及其团队,他们首次成功将成年体细胞重新编程为具有胚胎干细胞样多能性的细胞,这项突破性的工作获得了2012年诺贝尔生理学或医学奖。iPSC的制备不需要使用胚胎,而是通过转录因子的介入,将成体细胞(如皮肤细胞、血液细胞等)重新定向分化为各种类型细胞的多能干细胞。
iPSC被视为一次革命性的科学发现,为医学研究和临床应用带来了新希望和机遇。iPSC是一种可以从成体细胞中重新编程得到的多能干细胞,具有类似胚胎干细胞的多能性,但避免了使用胚胎的伦理争议。
什么是iPSC?
要了解iPSC,我们需要先了解什么是细胞重编程(Reprogramming cells)。所谓细胞重编程是指分化的细胞在特定条件下被逆转后恢复到全能性状态,或形成胚胎干细胞系,或进一步发育成一个新个体的过程。而细胞的分化是可逆的,山中伸弥通过病毒载体将四个转录因子(Oct4、Sox2、Klf4、c-Myc)的组合转入到已分化的体细胞中,使细胞重新编程,这个体细胞后来又可以变成类似胚胎干细胞的状态,从个体身上获取的体细胞进行诱导分化可以作为个性化方案治疗的筛选。所以,iPSC是将获得的成体细胞以病毒为载体,加入基因编辑,人为制造出具有多能性的干细胞,具备分化成人体各种组织、器官的能力,称为iPSC。
iPSC的临床研究
在clinical trial上以“iPSC”作为干预方式进行检索,一共有111项研究,涉及相关疾病的研究有25项,其中的病种包括难治性局灶性癫痫、黄斑变性、心衰、糖尿病视网膜病变等,具体见下表:
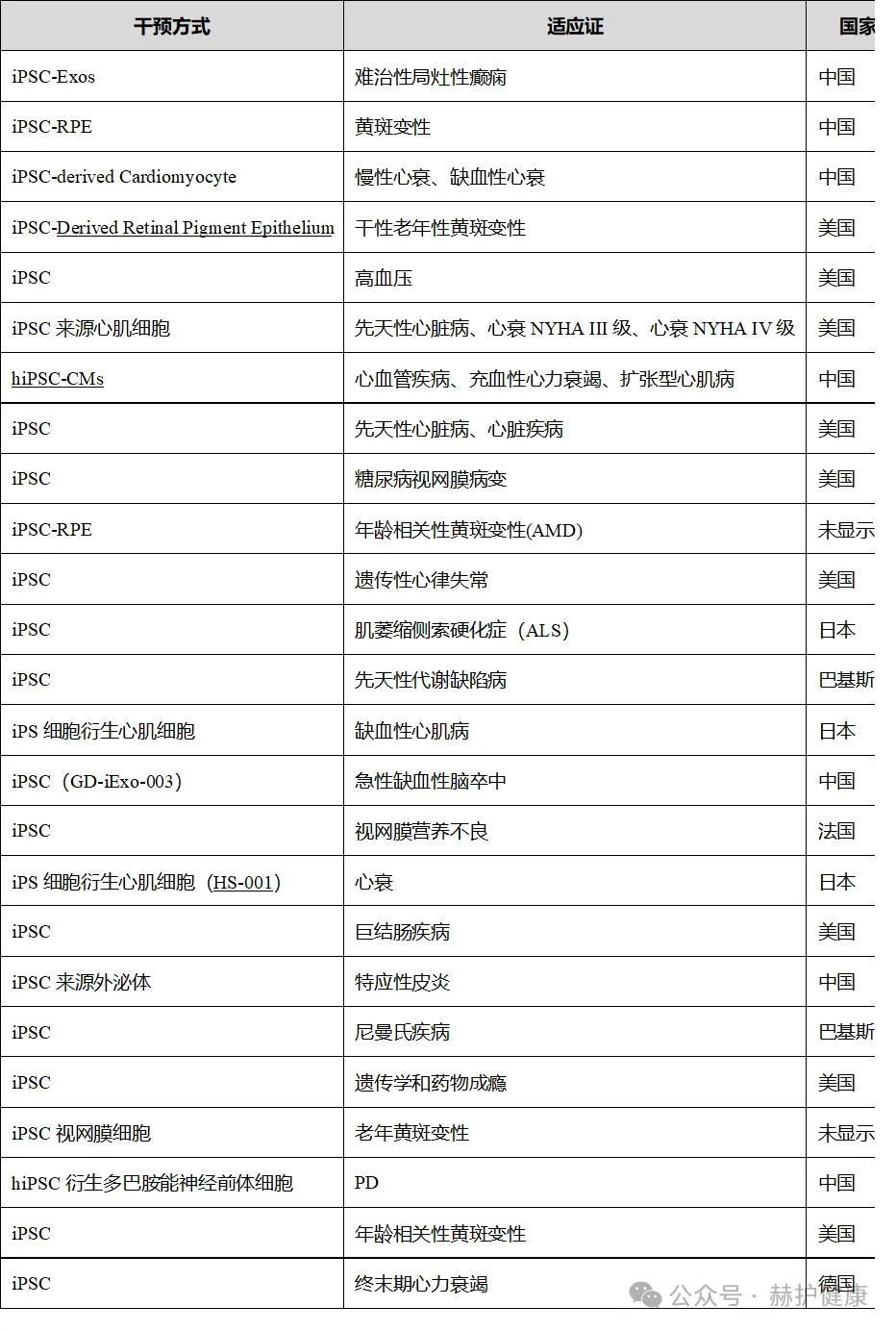
iPSC-RPE : induced pluripotent stem cell-derived retinal pigment epithelium
iPSC的应用前景
疾病建模与药物筛选: iPSC可以从患者自身获得,因此可用于模拟各种疾病的细胞模型,有助于深入了解疾病机制、筛选药物和个性化医疗方案开发。
再生医学和组织工程: iPSC可以用于生成各种细胞类型,包括心脏细胞、神经细胞、胰岛素β细胞等,为组织修复和再生医学提供了潜在细胞来源。
个体化治疗方法: 通过将患者的细胞转化为iPSC,并在体外分化成需要的细胞类型,可以为个体提供定制的治疗方案,提高治疗效果,降低排斥风险。
基因编辑与疾病治疗: 结合基因编辑技术,可以对iPSC进行精准的基因修正,用于治疗一些遗传性疾病,为基因治疗开辟新可能。
iPSC的未来发展方向
尽管iPSC已经取得了巨大成就,但仍然面临一些挑战和未知。未来的研究方向包括:
提高分化效率和纯度:进一步优化诱导和分化过程,提高iPSC向特定细胞类型的分化效率和纯度。
研究iPSC的长期稳定性:深入研究iPSC的遗传稳定性和安全性,确保其在长期应用中的可靠性。
探索新的治疗应用:拓展iPSC在更多疾病治疗和组织工程领域的应用,例如心血管疾病、神经退行性疾病等。
促进临床转化和标准化:加速iPSC从实验室研究到临床应用的转化,建立标准化的制备和应用流程。
iPSC虽然有多能性,但不完全等同于胚胎干细胞,目前通过重编程技术获得的iPSC还没有达到胚胎干细胞的全能状态,也就是所说的重编程不彻底。而通过逆转录病毒载体有产生肿瘤的风险。被重编程为iPSC所需时间较长,效率较低,距离iPSC走上正式临床应用还有一定的道路要走。