
诱导多能干细胞 (iPSC) 衍生的间充质干细胞 (iMSC) 为原代间充质干细胞 (MSC) 及其衍生物(尤其是细胞外囊泡 (EV))提供了一种有前途的替代品,可用于高级治疗药物。
新的研究证明,iMSCs 和 iMSCs-EVs 作为 MSC 衍生疗法的替代来源的巨大前景,因为它们具有强大的免疫调节和再生特性。
间充质干细胞 (MSC) 代表了一种干细胞群,在涉及组织再生和免疫系统的多种疾病中具有良好的治疗效果。
截至2024年9月30日,我国共有98款获准默许进入临床试验(临床试验默示许可)。2024年1月1日至9月30日共20款获准默许进入临床试验(临床试验默示许可),其中2024年第三季度新增3款,均为间充质干细胞来源。获批适应症:失代偿期肝硬化、糖尿病足溃疡、缺血性脑卒中、中重度系统性红斑狼疮等。
然而,与供体多样性、不同组织来源以及需要大量体外扩增有关的复杂性继续限制 MSC 作为先进治疗药物的使用。为了克服这些限制,必须确定不同的、可获得的 MSC 来源。诱导多能干细胞 (iPSC) 衍生的 MSC (iMSC) 的产生似乎提供了有效解决大多数这些限制的机会。作为多能干细胞的替代来源,iPSC 可以通过转录因子诱导的重编程从患者特异性成体体细胞(如皮肤成纤维细胞、外周血细胞或其他组织)中产生。此外,iPSC 被认为是 iMSC 的取之不尽的来源,可以满足高临床需求。
英国和澳大利亚的研究团队在自然杂志子刊Nat Med. 上发表的题为Production, safety and efficacy of iPSC-derived mesenchymal stromal cells in acute steroid-resistant graft versus host disease: a phase I, multicenter, open-label, dose-escalation study的研究成果证明,一个iPSC系可以生产 2900 万个临床剂量的 iMSC用于临床治疗。此外,从单个 iPSC 细胞或克隆诱导的 iMSC 在理论上更加均质。
2024年6月,上述团队在自然杂志子刊Nat Med. 上发表了题为Two-year safety outcomes of iPS cell-derived mesenchymal stromal cells in acute steroid-resistant graft-versus-host disease的研究成果,首次完成的iPS细胞衍生间充质干细胞(iMSC)的临床试验在15名患有类固醇抗性急性移植物抗宿主病的参与者中进行。在静脉输注iMSC后第100天评估期内报告了安全性、耐受性和有效性,结论是,iMSC的全身性输注是安全的,并且在2年的随访中耐受性良好,在首次输注后可持续达2年。ClinicalTrials.gov注册:NCT02923375。
重要的是,作为 MSC 的潜在无限来源,iMSC 在形态、免疫表型和三系分化能力方面与其原代组织来源的 MSC 非常相似。此外,已证明 iMSC具有更好的增殖能力,以及与组织来源的 MSC 相比在组织修复、免疫调节和分化应用方面的优势。如今,iPS细胞的研究进展较快,中国、美国、日本和其他国家至少有 50 项临床试验正在进行中。其中最有希望的一项是中国科学家使用 iPSC 逆转 1 型糖尿病,这是世界首创的突破,上个月《自然》杂志刚刚报道了这一突破。今年4月中国学者在Cell Discovery上报道iPSC技术治疗2型糖尿病,患者已被治愈。iPS细胞衍生的间充质干细胞具有强大的免疫调节和再生特性2024年10月15日,德国的研究人员在行业期刊Scientific Reports上发表了题为Unveiling the Immunomodulatory and regenerative potential of iPSC-derived mesenchymal stromal cells and their extracellular vesicles的研究成果,揭示 iPSC 衍生的间充质干细胞及其细胞外囊泡的免疫调节和再生潜力。

在过去的二十年中,多项研究表明, MSC 具有强大的临床应用潜力,因为它们通过细胞间相互作用以及释放可溶性因子和细胞外囊泡 (EVs) 发挥强大的免疫调节作用。
EVs是一类小的膜状纳米颗粒,可携带多种生物分子,包括蛋白质、脂质、核酸和小分子。有趣的是,EVs 在各种生理和病理过程中发挥着重要作用,例如细胞间通讯和免疫调节,并且被认为参与了多种疾病的进展,包括神经退行性疾病和心血管疾病。
最近,使用 MSC 衍生的 EVs 作为 MSCs 的治疗替代品越来越受欢迎,因为基于EV的疗法可以减轻与使用 MSCs 相关的安全问题。
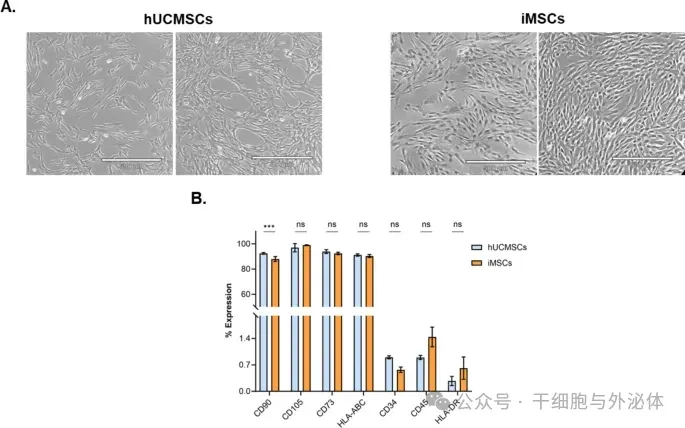
图:hUCMSCs 和 iMSCs 原代细胞的表征。(A)培养中 hUCMSCs(左图)和 iMSCs(右图)两种不同融合的代表性形态,比例尺为 500 μm。(B) hUCMSCs(蓝色条)和 iMSCs(橙色条)的免疫表型表征,以经典细胞表面标志子集的百分比表达表示,包括 CD90、CD105、CD73、HLA-ABC、CD34、CD45 和 HLA-DR(n = 3)。所有数据均以平均值 ± SD 表示。ns:不显著,***:p < 0.001,通过双向方差分析和 Sisak 多重比较检验。
iMSC 疗法比原发性 MSC 疗法具有更多优势,因为据报道 iMSC 在产生调节微环境的 EVs 方面更胜一筹。iMSC衍生的EVs 在许多疾病中的治疗效果已被探索,在伤口愈合、心血管疾病和肌肉骨骼病理学方面研究得最为透彻 。
为了全面比较 iMSC 和原代 MSC 的治疗效果,必须阐明它们的功能和潜在机制。为了进一步探索这一领域并解决现有的空白,德国的研究人员开发一个全面的基于细胞的检测平台。该平台旨在评估 iMSC 和 iMSC-EVs 的免疫调节潜力,包括几个特定的组成部分,以全面评估它们的效果:T 细胞增殖和巨噬细胞极化测定,以及 iMSC-EVs 在划痕试验中的再生潜力。
研究结果证明,诱导多能干细胞 (iPSC) 衍生的 MSC (iMSC) 的生成为解决限制 MSC 广泛应用为先进细胞疗法的大部分障碍提供了绝佳的机会。在该研究中,研究人员在体外细胞测定中比较了 iMSC 及其 EV 与人原代脐带衍生的 MSC (hUCMSC) 的治疗效果。结果证实符合 GMP 的 iPSC 可用于生成满足原代 MSC 表征标准的 iMSC,并且这些 iMSC 会释放真正的-EV。
随后,研究人员发现 iMSC 有效地发挥免疫调节潜力,可抑制 T 细胞增殖并诱导巨噬细胞极化向 M2 样表型,就像 hUCMSC 一样。此外,研究发现 iMSC-EVs 表现出与 iMSCs 细胞相似的显著免疫调节特性,进一步显示出与 hUCMSC 衍生的 EVs 相似的促再生潜力。另外,这项研究首次提供了促炎性 iMSC 预处理的证据,这是一种可行且引人注目的策略,可增强 iMSC-EVs 对人体免疫细胞的免疫调节作用。