
人类诱导多能干细胞 (hiPSC) 源自重编程的成人体细胞,在疾病建模、个性化医疗、药物研发和再生疗法方面具有重大前景。
人类诱导性多能干细胞 (hiPSC) 是由成人体细胞(例如皮肤成纤维细胞或血细胞)通过基因重编程到胚胎状态而产生的。当编码特定转录因子的基因被引入成体细胞时,它们会获得干细胞状态的关键特征,即分化成几乎所有细胞类型和自我更新的能力。hiPSC 于 2007 年在日本首次报道,当时山中伸弥教授重编程了小鼠成纤维细胞,随后又重编程了人类成纤维细胞。由于 hiPSC 具有多能干细胞状态,因此可以为研究和治疗应用提供无限量的各种患者特异性细胞。
hiPSC 在再生医学领域的细胞疗法中前景广阔,可为目前尚无可行治疗方法的多种疾病提供治愈或有效治疗。重要的是,hiPSC 可提供几乎无限的干细胞供应,因为它们能够分化成任何类型的细胞,并且具有无限增殖的潜力。
hiPSC 的发现克服了与人类胚胎干细胞 (hESC) 相关的伦理问题,hESC 可从 5 至 7 天大的囊胚的内细胞团中提取,其生产需要破坏人类胚胎。hESC 被认为是多能干细胞的黄金标准,但由于人们有不同的科学、宗教和道德信仰,其研究与许多公共和政治争议有关;此外,这些早期胚胎的使用在支持生命运动的人士和反对干细胞研究的人士中引起了很多争论和争议。
在干细胞研究领域,21 世纪初,从胎儿和成人来源(如羊水和脐带血)分离的人类多能干细胞被提议用于研究和临床应用,因为它们不会引起任何特殊的伦理问题。然而,这些细胞是否可以无限扩增,最重要的是,它们是否具有多能性,即是否有潜力分化为三个胚层中的任何一个,仍然存在争议。
hiPSC 结合了 hESC 和成体干细胞的最佳特性,避免了大多数伦理争议,因为无需使用胚胎或卵母细胞来生成 hiPSC。值得注意的是,它们提供了几乎无限的干细胞或免疫细胞来源,因为它们可以无限繁殖,并且具有分化成任何细胞类型的内在潜力。出于这些原因,hiPSC 在疾病建模、个性化治疗、药物发现和再生医学方面具有巨大潜力。
如今,hiPSC 可从多种细胞来源获得,包括脐带血、外周血等。重编程技术的重大进步,例如仙台病毒介导的重编程和蛋白、化学等非病毒方法,提高了 hiPSC 生成的效率和安全性。这些方法促进了体细胞向多能状态的转化,从而拓展了其在再生医学和个性化治疗中的多种应用潜力。
使用患者来源的 hiPSC 可以提供大量与疾病相关的细胞,甚至包括难以接近的细胞,例如神经元和心肌细胞,用于疾病建模,以研究人类疾病的病因和制定治疗策略。
此外,由于 hiPSC 可以从患者本身获得,基因组编辑技术的快速发展可能允许纠正患者来源的 hiPSC 中致病基因突变或将特定突变引入来自健康供体的细胞中。
hiPSC助力药物研发更有效、更安全
关于 hiPSC 在药物研发中的应用,值得一提的是,鉴定一种成功的治疗药物需要大量的测试,而药物研发的失败率甚至超过 90%,因此是一个漫长、高风险且昂贵的过程。因此,hiPSC 培养的可扩展性及其无限复制而不经历复制性衰老的能力使疾病表型能够在培养规模上一致地重现,以满足药物筛选的需求。
自 1938 年以来,动物试验一直是监管要求,目的是在药物进入临床试验之前确定其安全性和有效性。尽管动物模型揭示了许多疾病机制,但动物和人类之间的生理和遗传差异常常导致临床试验失败,并带来严重后果。2007 年至 2010 年间,66% 的 III 期失败是由于缺乏疗效,21% 是由于药物毒性,这凸显了改进临床前评估和临床候选药物预测数据的必要性。
然而,最近的数据显示,预测准确性方面的这种差距仍然存在。对 221 项动物实验的审查发现,只有 50% 的结果与后来的人体研究一致,动物试验仍然无法预测 I 期试验和上市后早期撤回期间近一半药物的毒性。
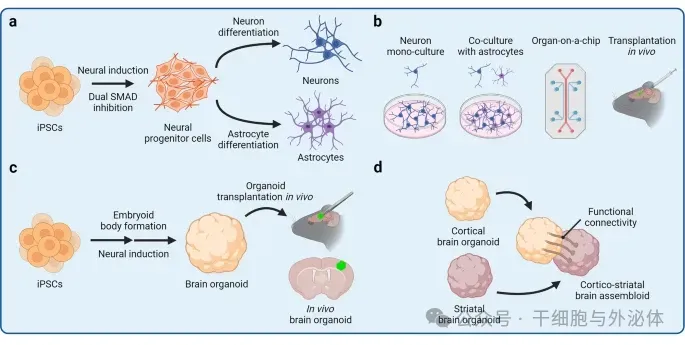
图:hiPSC) 衍生的细胞模型
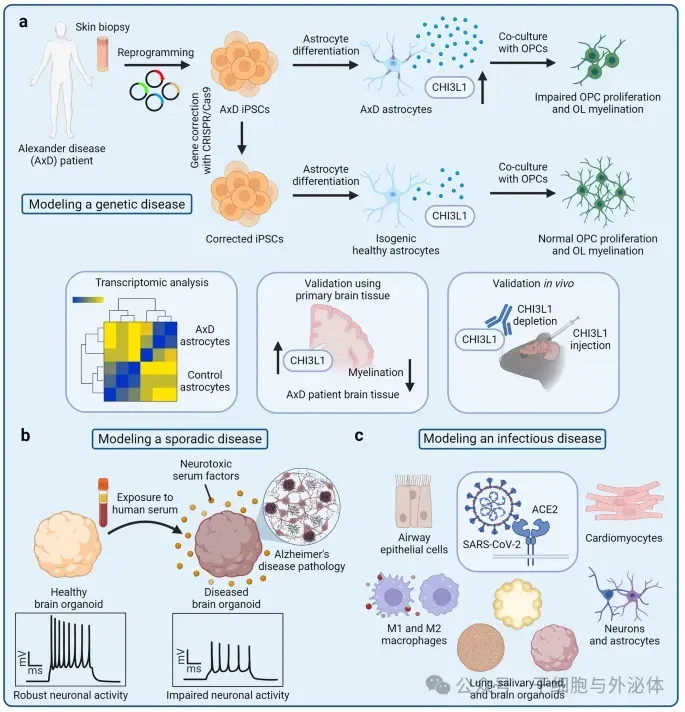
图:使用 hiPSC 衍生细胞进行疾病建模
FDA 现代化法案 2.0 4已于 2022 年 12 月由参议院和众议院通过,授权使用替代测试平台,并取消某些药物进入临床试验前进行动物测试的要求。目标是提高临床前安全性和有效性评估的预测性,并减少药物发现和开发计划中对动物的使用。
新法规为制药公司和研究人员探索药物研发的创新方法提供了重大机遇。它将加速创新,并更快地将更安全、更有效的药物推向市场。
FDA 现代化法案 2.0 的一项关键规定是鼓励使用与人类相关的体外模型,例如人类诱导性多能干细胞 (hiPSC),这些模型可以更好地代表人类生理学和疾病表型。hiPSC已成为临床前药物开发中动物试验的有力替代品,因为它们保留了遗传背景并可以模拟特定的疾病表型。
hiPSC 技术已经促进了更高效的药物开发,并已用于 35 多个神经退行性疾病临床试验。在临床前靶点识别和评估中使用人体生物学可提高临床前药物开发的准确性和速度,减少动物试验次数,并增加临床试验成功的机会。
hiPSC细胞疗法:从糖尿病到癌症治疗
在再生医学领域,hiPSC 有望用于治疗多种目前尚无治愈方法或有效疗法的疾病。将 hiPSC 用于细胞治疗的基本模式是首先将它们分化为所需的目标细胞类型,然后将产生的专门的组织特异性细胞移植到患者体内。
细胞疗法最近成为一种有前途的方法,可以修复或替换受损组织以及设计对癌症等疾病的免疫反应。
虽然可以从患者体内分离出原代细胞,例如 T 细胞、自然杀伤 (NK) 细胞和间充质干细胞,然后用作自体细胞疗法,但其他类型的细胞,如神经元,不能用于移植。此外,原代细胞的质量可能因疾病或种系突变而受损,并表现出不必要的异质性。由于 iPSC 可以通过基因工程改造、克隆扩增并分化为大多数人体细胞类型,因此 iPSC 技术可用于克服这些限制。
基于 hiPSC 的细胞疗法可分为两类——自体和同种异体。在自体细胞疗法中, hiPSC来自接受细胞移植的同一患者。自体细胞疗法旨在防止接受者对移植产生免疫排斥,因为免疫系统将移植的细胞识别为“自身”组织。首先从将接受自体细胞疗法的患者身上采集组织活检,然后将分离的体细胞重新编程为hiPSC。然后可以对这些hiPSC 进行基因改造,以纠正不良突变或引入新的基因表达。
在同种异体细胞疗法中,来自通用供体的 iPSC 用于移植,从而避免了从每个接受细胞移植的患者身上生产 iPSC 的漫长而昂贵的过程。所需细胞可以提前分化、表征和储存,以便细胞产品可按需提供或“现成”供应,而无需内部生产。
(1)hiPSC衍生的胰岛功能性治愈 1 型糖尿病患者
近期来自北京大学邓宏魁教授的研究小组在《细胞》杂志上发表了他们的研究成果,他们从患者体内提取细胞,利化学的方法生成hiPSC,并使其生长为胰岛,然后将其注射回患者的腹部。
图:胰腺中的胰岛细胞
在大约持续 30 分钟的手术中,研究人员将他们培育的 150 万个胰岛注射到第一位患者(一位 25 岁的女性)的腹部。将它们放入腹部便于监测并在必要时取出。两个半月后,测试显示患者自身产生的胰岛素足以停止注射。
一年后,她仍在自行产生胰岛素。研究小组指出,由于之前接受过肝移植,该患者已开始接受免疫抑制药物治疗;因此,目前尚不清楚她的免疫系统是否会复制最初导致她患上 1 型糖尿病的攻击类型。目前该团队正在开展2型糖尿病的临床研究。
(2)hiPSC衍生的免疫细胞用于治疗癌症
宫颈癌是全球女性最常见的恶性肿瘤之一。不幸的是,这种预防措施对已确诊的癌症无效,一旦癌症转移或复发,通常无法治愈。
幸运的是,科学家在开发一种有前景的宫颈癌治疗策略方面取得了重大进展:再生细胞毒性 T 淋巴细胞 (rejTs)。这些淋巴细胞可以经过改造,以针对主要在宫颈癌细胞中表达的 HPV 特异性抗原,从而构成一种靶向免疫疗法。理想情况下,rejTs 应由从患者自身采集的诱导多能干细胞(hiPSC)产生。
在此背景下,日本顺天堂大学医学院首席教授安藤美纪、研究生古川芳树和助理教授石井绿的研究团队最近取得了突破,开发出用于治疗宫颈癌的强大的 iPSC 衍生 rejT。他们的研究成果于 2023 年 12 月 12 日在Cell Reports Medicine上在线发表。
Fate Therapeutics, Inc.(纳斯达克股票代码:FATE)是一家临床阶段生物制药公司,致力于为癌症和自身免疫性疾病患者提供一流的诱导多能干细胞 (iPSC) 衍生的细胞免疫疗法。2024 年 5月该公司公布了针对 CD19 的 iPSC 衍生 CAR-NK 细胞候选产品临床前数据,FT522用于治疗复发或难治性 B 细胞淋巴瘤,包括非霍奇金淋巴瘤、滤泡性淋巴瘤等。
另外,hiPSC 衍生免疫细胞的新进展产生了强大的 iNK 和 iT 细胞,它们在动物模型和临床试验中表现出对癌细胞的强大杀伤力。
建立hiPSC资源库,惠及更多大众
原则上,hiPSC 可以直接从需要治疗的个体患者身上提取;这一程序的优势在于确保相同的免疫状态,并将移植排斥的风险降至最低。
然而,为个体患者生产自体临床级细胞将带来巨大的时间成本和科学困难,大规模应用可能会在经济上受到限制。个性化 hiPSC 疗法的替代方法是创建一个临床级 hiPSC 资源库,这些系可以扩增和分化,供大量患者使用 。
理想情况下,这样的hiPSC资源库将由从健康的 O 型血志愿捐献者身上获得的 hiPSC 组成,这些捐献者的选择是为了最大限度地提高人类白细胞抗原匹配的机会,从而最大限度地降低同种异体移植排斥的风险。
假设单个多能干细胞系可以为大量潜在接受者提供细胞或组织,日本、英国等一些研究已经开展,以计算需要多少 hiPSC 捐赠者才能覆盖不同国家的足够人口;因此,来自单个捐赠者的细胞可以永远冻存,并可被每个人用于不同的细胞医疗。例如,在日本,建立了一个由 7 名供体提供的 27 个 iPSC 系组成的单倍体库,可匹配约 40% 的日本人口。
2024年 10 月29日,专门从事人类诱导多能干细胞 (hiPSC) 和hiPSC 衍生细胞疗法公司I Peace, inc. 宣布已成功生成 HLA A、C 和 DPA1 纯合的 hiPS 细胞系。两种克隆系可供细胞疗法开发商和制药公司作为 GMP 和研究级的现成产品使用。该细胞系为 HLA A、C 和 DPA1 纯合子。美国有超过 1 亿人(35.91%)拥有这种 HLA A 单倍型。
总之,hiPSC 的发现对细胞和基因治疗领域产生了深远的影响,从糖尿病到癌症治疗,hiPSC成为再生医学中细胞治疗的宝贵细胞来源。