
来源:BioArtMED
抑郁症和老年痴呆症分别是年轻人和老年人群中最为常见的重大脑疾病,目前临床上严重缺乏对这两种重大脑疾病的治疗手段。许多长程的临床追踪研究表明,早年发生过抑郁症的人会显著增加晚年患老年痴呆症的风险,表明抑郁症是促进老年痴呆症发生的独立风险因素。然而,尽管抑郁症与老年痴呆症之间的临床相关性已经被报道多年,但抑郁症促进老年痴呆发症生的细胞分子机制尚不清楚。
钙稳态调节蛋白 (CALHM) 是一种具有四次跨膜结构的电压依赖的钙离子通道,同时也是介导细胞ATP释放的重要通道。因此,CALHM蛋白在维持哺乳动物生理功能等方面具有重要作用。已有研究表明,CALHM蛋白功能紊乱会导致多种神经精神疾病的发生,包括抑郁症和阿尔茨海默病(AD,老年痴呆症的主要形式)。军事医学研究院袁增强课题组长期致力于CALHM蛋白功能的研究,首次发现Calhm2蛋白是一种钙依赖的ATP释放通道,并且发现其在抑郁症样小鼠模型大脑中显著降低,Calhm2的缺少会导致大脑中星形胶质细胞ATP 释放显著减少,进而导致小鼠的抑郁样行为(Ma et al., Mol Psychiatry. 2018);发现Calhm2 Q87A突变会显著增加抑郁症的易感性,并总结了星形胶质细胞在抑郁和AD中的作用(Liao et al., PIBB. 2021; Liao et al., Front Med. 2021);此外,袁增强团队还发现Calhm2与AD的发生密切相关,小胶质细胞特异性敲除Calhm2可以减轻5XFAD小鼠的神经炎症,进而改善AD小鼠的认知功能(Cheng et al., Sci. Adv. 2021)。这些研究结果提示,Calhm2可能是连接抑郁症和老年痴呆症的重要靶点。
近日,军事医学研究院袁增强课题组在AD领域顶级杂志Alzheimer’s & Dementia上在线发表了题为CALHM2 V136G polymorphism reduces astrocytic ATP release and is associated with depressive symptoms and Alzheimer’s disease risk的研究成果,发现CALHM2 V136G突变通过调节星形胶质细胞ATP释放参与抑郁症和老年痴呆症发生的过程,首次揭示的抑郁症作为独立风险因素促进AD发生的细胞和分子机制,为抑郁症和AD的共病治疗提供了潜在药物靶点。

在该研究中,袁增强团队和浙江大学附属第二医院吴志英团队合作,通过对中国汉族人群AD患者样本的单核苷酸多态性 (SNP) 测序分析发现,CALHM2中的SNP rs232660在中国汉族人群的AD患者中显著增加(约2倍),该SNP rs232660导致第136位氨基酸位点的缬氨酸被替换为甘氨酸 (V136G)。进一步研究发现,V136G突变破坏了CALHM2蛋白的ATP释放通道特性,是一种功能缺失型突变(loss of function)。通过序列比对发现,CALHM2在人和小鼠等多种物种中高度保守。为进一步研究该突变的在体功能,研究人员构建了Calhm2 V136G敲入(knock in)小鼠。利用多种细胞、分子生化以及动物行为学检测等实验方法,研究人员发现V136G突变导致了星形胶质细胞ATP释放的减少,进而导致小鼠的抑郁样行为;外源补充ATP可以显著缓解Calhm2 V136G突变小鼠的抑郁样行为。更重要的是,研究人员发现,与正常小鼠相比,长期处于抑郁状态的Calhm2 V136G小鼠在老年时(18月龄)会出现更严重的认知功能障碍。这些发现提示,CALHM2可能是连接抑郁症和老年痴呆症的关键靶点,解释了抑郁症作为独立风险因素促进老年痴呆症发生的重要临床现象。
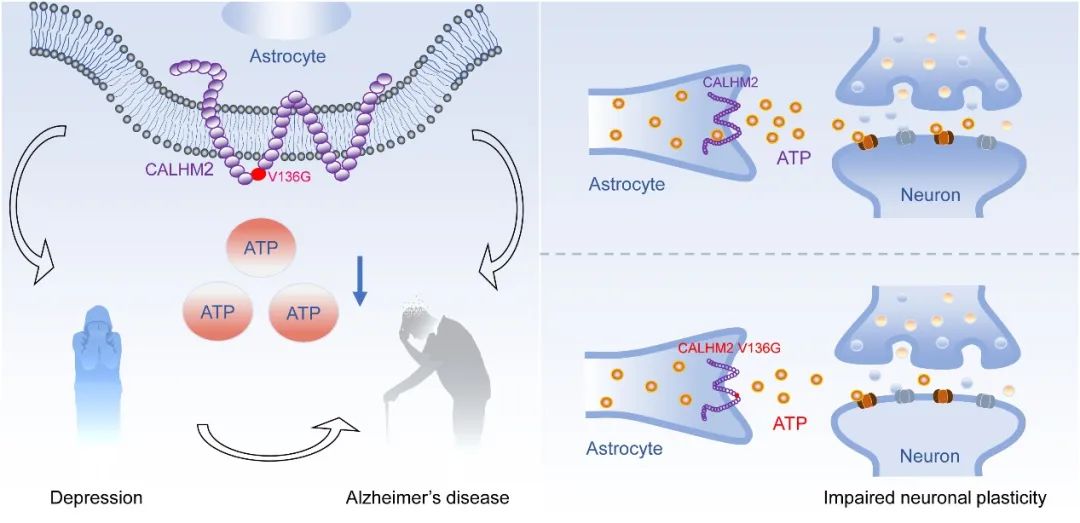 图1. CALHM2 V136G参与抑郁症和AD发生发展模式图
图1. CALHM2 V136G参与抑郁症和AD发生发展模式图
军事医学研究院袁增强研究员和南方医科大学潘瑞远教授(袁增强课题组前博士后)为该工作的共同通讯作者,袁增强课题组硕士生廖洋(已毕业,现为中南大学博士生)、博士研究生王英燚以及浙江大学附属第二医院陶青青主任为共同第一作者。
原文链接:https://doi.org/10.1002/alz.13366