
糖尿病是常见病、多发病,是严重威胁人类健康的世界性公共卫生问题。糖尿病多数起病隐匿,症状相对较轻,半数以上病人可长期无任何症状,威胁着全球约5.37亿人的身心健康,中国就有1.3亿糖尿病患者,而且发病率呈逐年上升趋势,预计到2030年,患病人数将飙升至6.43亿人!
鉴于现有治疗手段的局限性,研究人员近年将目光锁定在再生疗法中。值得欣慰的是,近期糖尿病领域再次传来好消息,中国和外国又有突破性进展!
01 糖尿病
1型和2型糖尿病大不相同
糖尿病(DM)是一种严重且高发的慢性代谢性疾病,其特征是绝对或相对胰岛素缺乏或胰岛素抵抗。目前临床上应用最广泛、 最被公认的糖尿病病因分型方法为1997年美国糖尿病学会(ADA)和1999年世界卫生组织(WHO)提出的建议:根据病因分型,可将糖尿病分为1型糖尿病(T1DM)、2型糖尿病(T2DM)、特殊类型糖尿病和妊娠期糖尿病(GDM)。
后续不同的学术组织及不同的专家共识对糖尿病的分型有不同的建议,具体如下表:
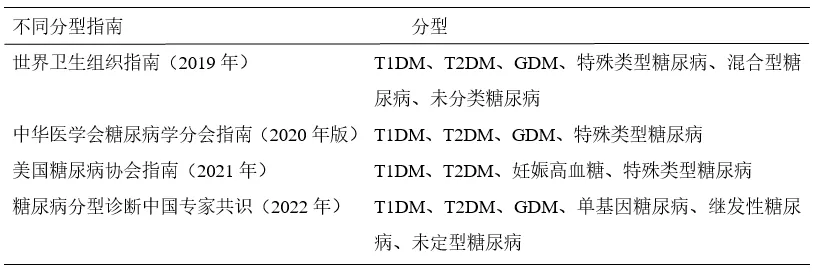
1型糖尿病(T1DM)
1型糖尿病,是由于免疫系统发育不良或免疫应激引发的糖尿病,又名胰岛素依赖型糖尿病(I1DM)或青少年糖尿病,易出现糖尿病酮症酸中毒(DKA),又叫青年发病型糖尿病,这是因为它常常在35岁以前发病,占糖尿病的10%以下。
1型糖尿病患者通常需要每天注射胰岛素,来补充未产生的胰岛素,也就是说患者从发病开始就需使用胰岛素治疗,并且终身使用。

2型糖尿病(T2DM)
2型糖尿病是最常见的糖尿病类型,由于多发于成年,又称成人发病型糖尿病。该病主要由胰岛素抵抗、胰腺β细胞分泌功能障碍所致,约占所有糖尿病患者的85%~95%。约30%的2型糖尿病患者,需要注射胰岛素来控制病情。

糖尿病的可怕并不在于血糖本身,而是长期高血糖导致心脑血管、肾病、眼病、神经病变等致畸、致残的风险。
并发症高达100多种,常见的慢性并发症有6种:糖尿病心血管并发症、糖尿病性脑血管病、糖尿病肾病、糖尿病眼部并发症、糖尿病足、糖尿病神经病变。糖尿病的急性并发症包括糖尿病酮症酸中毒、高渗性高血糖、乳酸性酸中毒。
02 糖尿病细胞治疗

中外近期更新糖尿病细胞治疗领域两大突破进展!
干细胞治疗糖尿病是一种新型的治疗方法,它涉及到将干细胞注入患者体内,以促进胰岛素的分泌,从而达到治疗糖尿病的目的。
干细胞是一类具有自我复制和多向分化潜能的原始细胞,它们在一定的诱导条件下可以分化成多种功能细胞或组织器官。由于这种独特的特性,医学界有时称它们为“万用细胞”。
在糖尿病治疗中,科学家们通常会使用以下几种类型的干细胞:
● 间充质干细胞(MSCs):可以从骨髓、脂肪组织、脐带血等多种组织中提取,它们具有免疫调节和抗炎作用,能够改善胰岛β细胞的环境,减少自身免疫攻击,并有助于受损细胞的修复。
● 胚胎干细胞(ESCs):具有全能性,可以分化成任何类型的细胞。然而,它们的使用涉及伦理问题,并且在提取过程中可能会破坏胚胎。
● 诱导多能干细胞(iPSCs):通过将成熟细胞重编程为干细胞状态,可以避免使用胚胎干细胞的伦理问题。它们同样具有分化成各种细胞类型的能力。
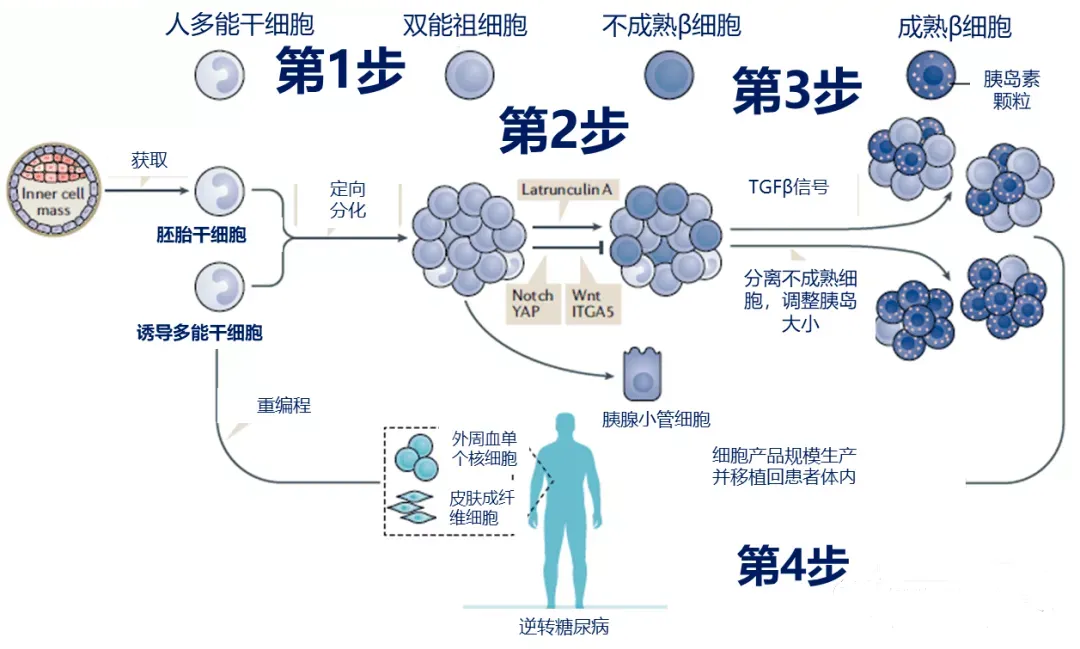
2型糖尿病曙光:中国首个基因修饰间充质干细胞1类新药IND获批
2024年8月28日,国家药品监督管理局药品审评中心(CDE)批准了吉源生物的“人GLP-1和FGF21双因子高表达脂肪干细胞注射液”的新药临床试验申请(IND),适应症为2型糖尿病,这是我国首个基因修饰干细胞获准进入临床备案。
该疗法是利用基因修饰技术,对脂肪干细胞进行高效改造,使其在患者体内表达两种重要的代谢调节因子,即胰高血糖素样肽-1(GLP-1)、成纤维细胞生长因子21(FGF-21),其终极目的是通过调节这两种引子,来改善胰岛功能、调节血糖、控制体重,最终达到治疗2型糖尿病的目的。
注:GLP-1,是肠道分泌的一种激素,在刺激胰岛素分泌、抑制胰高血糖素分泌、延缓胃排空速度等方面发挥作用,已成为2型糖尿病治疗的重要靶点。
FGF-21,一种由肝脏合成的关键糖脂代谢调节分子,具有改善胰岛素敏感性、调节脂肪代谢、降低血糖等功能。将这两个重要代谢调控因子高效表达在脂肪间充质干细胞上,可以实现对糖脂代谢的协同调节,同时利用干细胞的归巢特性,能够靶向作用于相关组织器官,有助于保护胰岛β细胞,阻止并发症的发生。
据悉,该项目临床研究将由上海交通大学医学院附属瑞金医院进行,中国工程院院士宁光教授作为主要研究者。这项研究标志着中国在基因修饰间充质干细胞(MSC)药物研发领域,迈出了重要的一步,为2型糖尿病患者带来了新的曙光!
新型诱导性多能干细胞胰岛替代疗法(细胞袋),助1型糖尿病患者4年未用胰岛素
● Sernova细胞袋:新型诱导性多能干细胞(iPSC)胰岛替代疗法
Sernova细胞袋是位于加拿大的再生医学治疗公司Serrova Corp与芝加哥大学医学院合作研发的一种可植入的现成诱导性多能干细胞(iPSC)胰岛替代疗法。
该疗法的治疗原理是,利用微创技术,将这种小型的植入式医疗设备,植入患者腹部肌肉的皮下,植入细胞袋约6周后,通过免疫抑制疗法稳定病情,然后将胰岛细胞移植到细胞袋形成的血管化组织腔中。由于该设备是多孔的,植入后会在体内形成天然的血管化组织环境,使治疗细胞能够长期存活和发挥作用,释放出糖尿病患者所缺乏或缺乏的必需因子,适用于胰岛素依赖型糖尿病(1型糖尿病)的治疗。
● 2024欧洲糖尿病研究协会:Ⅰ/Ⅱ期临床研究结果喜人!
2024年9月12日,Sernova细胞袋的第一批Ⅰ/Ⅱ期临床试验(NCT03513939)结果,已在2024年欧洲糖尿病研究协会(EASD)年会上公布。该研究入组的是18~65岁的1型糖尿病患者,病史超5年,且有严重的低血糖发作和低血糖无意识病史,意味着他们在危险的低血糖情况下无法察觉风险。入组后将患者分为两组,A组(6例,接受第一代细胞袋治疗)、B组(7例,接受胰岛容量增加50%的细胞袋治疗)。
结果表明,A组的所有患者在治疗后都实现了长期不再需要外源胰岛素治疗的目标。特别是其中一位患者已经连续四年不需要注射胰岛素,血糖水平维持在非糖尿病的正常范围内。所有这些患者的糖化血红蛋白(HbA1c)水平都控制在6.5%或以下,而参考值显示,非糖尿病患者的HbA1c通常在5.7%至6.4%之间。
总的来说,通过干细胞技术生成功能性胰岛β细胞,结合细胞封装技术将这些细胞植入患者体内,不仅可以替代传统的胰岛素注射,还能够有效避免免疫排斥反应。这种联合应用有望突破当前治疗的限制,提供一种安全、有效且可能永久性的治疗方案,从根本上改变1型糖尿病患者的生活质量!
糖尿病是一种困扰无数患者身体健康的代谢性疾病,患者不仅需要长期用药治疗,由此引发的并发症,如糖尿病足、糖尿病肾病等,更是严重威胁患者的身心健康。随着干细胞等再生医学的不断发展,研究人员渴望从细胞层面寻求解决办法。
虽然干细胞治疗糖尿病仍处于早期阶段,但近年国内外越来越多的研究,已证实了干细胞疗法治疗糖尿病的有效性及安全性,为糖尿病患者带来了新的希望与选择!