
来源:BioArtMED
细胞疗法是治疗帕金森病(Parkinson’s disease,简称PD)的良好方法,因为其发病机制相对简单,即中脑黑质致密部位(substantia nigra pars compacta region)的多巴胺能神经元局部退化。在动物实验和人类试验中,移植人类胎儿腹侧中脑组织(ventral mesencephalon tissues )或细胞后可以在一定程度声恢复运动功能,但结果的平行性较差,这说明此类细胞疗法需要改进,以确保获得的中脑多巴胺能(midbrain dopaminergic,简称mDA)细胞数量充足、制备和移植程序标准。
最近的技术进步使得从人类多能干细胞(human pluripotent stem cells,简称hPSCs),如胚胎干细胞(embryonic stem cells,简称ESCs)和诱导多能干细胞(induced pluripotent stem cells,简称iPSCs),有效地生成mDA神经元成为可能,为建立PD的hPSC基移植疗法奠定了基础。多项研究已经证实,在移植到帕金森病动物模型中时,hPSC来源的mDA前体细胞能够很好地整合到宿主大脑中,并发育成熟为功能性的mDA神经元,显著改善了运动功能。此外,最近的一项开创性研究报告称,接受自体移植的hiPSC来源的mDA前体细胞的PD患者在植入后24个月内表现出稳定或改善的临床症状。目前, hiPSC来源的(UMIN000033564,日本)和hESC来源的(NCT04802733,美国;NCT05635409,欧盟)mDA前体细胞最近已进入早期临床试验阶段。
将PD的细胞移植引入临床的第一个关键步骤是精准完备的定义细胞产品特性。尤其直观重要的是,确立细胞采用临床级别材料,遵循GMP(good manufacturing practice)标准进行生产,并且符合临床应用标准。随后,临床前研究应通过大规模动物实验提供疗效的有力证据,并系统、长期地关注安全相关问题,如毒性、生物体内分布以及致瘤性。此外,临床前研究需要建立用于移植细胞剂量的最佳范围,作为临床试验的参考。最重要的是,研究设计必须谨慎,并且结果必须以无偏见的方式进行评估。这通常需要与第三方合作,并全程接受监管。
2023年12月11日,来自韩国延世大学医学院的Dong-Wook Kim和高丽大学Dae-Sung Kim合作在Cell Stem Cell上发表题为Preclinical and dose-ranging assessment of hESC- derived dopaminergic progenitors for a clinical trial on Parkinson’s disease的文章,展示了一项旨在将hESC来源的mDA神经元引入治疗PD的人体试验的临床前研究的过程和结果。

该研究中细胞分化方法已经针对临床应用进行了优化,确保符合GMP标准。这种优化方法使得大规模生产高纯度、可冷冻保存的mDA前体细胞成为可能,同时保持了严格的质量控制(QC)。由独立CRO使用免疫缺陷大鼠进行的1年长期大规模移植研究表明,此外,临床mDA前体细胞表现出治疗潜力,并在毒素诱导的半帕金森大鼠中产生了治疗效果的剂量范围。这些发现提供了关于人体试验中适当的细胞剂量的重要信息。
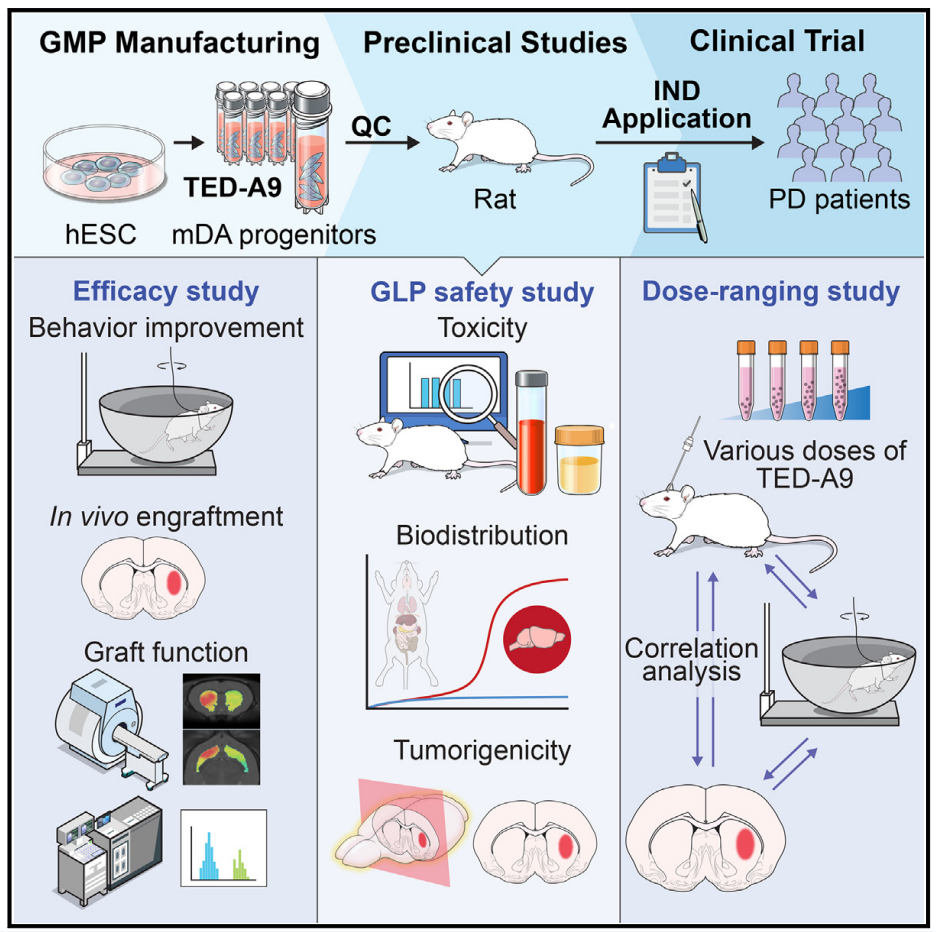
hESC来源的mDA细胞移植在治疗PD等方面颇具临床前景。作者在严格的GMP条件下,优化了mDA制备方法,并大规模制备了临床级别的hESCs,并从中获得了高纯度、可冷冻保存的mDA前体细胞。作者还在符合GLP(good laboratory practice)的设施中评估了这些细胞的毒性、生物体内分布和致瘤性。在第三方机构中,不同剂量的mDA前体细胞被移植到帕金森大鼠体内,观测时程长达一年。结果显示,移植的mDA神经元不具有致瘤性、显著毒性以及除注射部位外的异位整合。并观察到明显的剂量依赖性行为改善,最小有效剂量范围为5,000至10,000个mDA前体细胞。这些结果为确定人体临床试验的最低细胞剂量(315万个细胞)提供了有力依据。
基于上述结果,作者获得了韩国食品药品安全部的PD细胞疗法1/2a期临床试验批准,并已经开展临床试验。
原文链接:https://doi.org/10.1016/j.stem.2023.11.009