
来源:医麦客
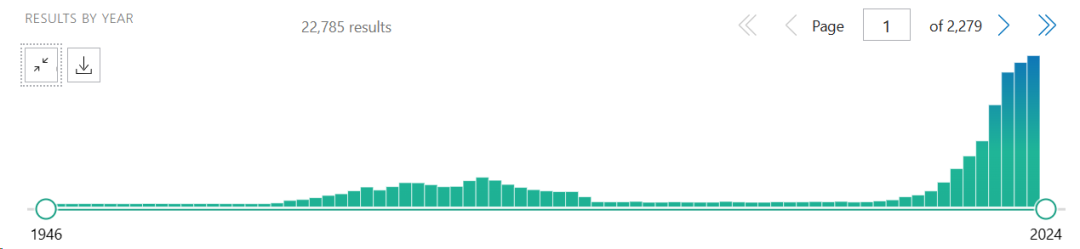
类器官(Organoids)相较于传统的2D细胞培养模型相比,能够更好地模拟生理病理状态和器官组织的发生过程,弥补了现有模型的局限性,已经被广泛用于肿瘤研究、疾病建模、药物筛选、再生医学、精准医学等领域。据PubMed数据显示,近年来,类器官的相关研究呈逐年递增趋势,成为一大热门前沿赛道。
一篇文章曾报道了利用同种异体诱导多能干细胞(iPSC)衍生的软骨类器官治疗关节软骨缺损的研究。科研人员利用iPSC产生由软骨细胞和细胞外基质(ECM)组成的软骨,并将其转移到三维培养物中进一步培养,以使衍生的软骨产生ECM并在周围累积以形成软骨组织颗粒。从理论上来说,由于iPSC的自我更新活性,异源iPSC衍生的软骨组织可以无限生产并移植到无限数量患者体内以解决供体缺乏、疾病传播、质量差异的问题,不过目前实现起来仍有困难。
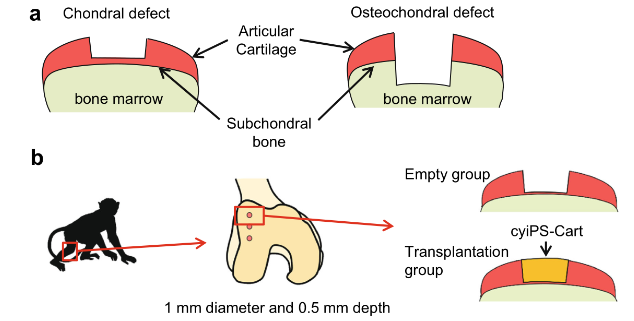
▲ 灵长动物类器官移植
截止文章发表,尚未有评估过同种异体软骨移植到灵长类动物模型中的研究,而这项研究深入分析了在不使用免疫抑制药物的情况下iPSC衍生的软骨类器官的同种异体移植。结果显示,同种异体iPSC衍生的软骨类器官在膝关节软骨缺损的灵长类动物模型中存活、整合并重塑为关节软骨,并未引起免疫反应,有助于组织修复至少4个月。移植的软骨类器官与宿主天然关节软骨整合,并防止周围软骨的退化。针对移植体的单细胞RNA测序和分子生物学分析表明,SIK3、PRG4和细胞分化相关通路参与移植后的软骨重塑及修复过程。
这一研究结果表明,iPSC衍生的软骨类器官的同种异体移植可能在临床上适用于治疗关节软骨缺损的患者。
类器官移植治疗潜力初显
类器官被用于移植到其他生命体中以评估再生能力的研究为类器官在再生医学中的应用铺平了道路。相较于植入式医疗设备,类器官具有功能更加多样化、排斥更小、不易受磁场或物理影响等优点,同时,类器官还可以通过用恢复的组织替换受损器官来在遗传基因异常的情况下进行基因校正。目前,已有不少研究报道了类器官在再生医学/器官移植方面的应用潜力。
近期,《Cell Stem Cell》上的文章报道了来自美国辛辛那提儿童医院的研究人员培养了多能干细胞衍生的人结肠类器官(HCO),发育出了造血内皮样细胞和相关的RUNX1+细胞、红骨髓祖细胞等,且最终产生功能性常驻型巨噬细胞。移植到小鼠体内后,HCO巨噬细胞保留在结肠类器官组织内,不会被宿主骨髓来源的巨噬细胞取代。这个项目为生产含有常驻免疫细胞的人体类器官的研究作了铺垫。
去年7月,日本东京医科齿科大学研究团队首次实施了干细胞衍生类器官移植人体的临床研究,他们对一例难治性溃疡性大肠炎患者移植了使用患者自身健康的肠道黏膜干细胞培养的类器官。将类器官移植到大肠病患处,再覆盖上可在人体内降解的薄膜加以固定利用患者自身的组织来修复黏膜。患者在接受治疗后状态良好。
此前,在《Science》的一篇研究报道中,科研人员培育了一种类似胆管的类器官,并将其移植到胆管受到化学损伤的小鼠体内,其能够跟宿主细胞融合,再生受损组织,相较于对照组而言,小鼠的生存期得到大大延长。而后,研究人员又培养了新的人类器官组织并体外移植到三个捐赠的人肝脏中,这些类器官能够修复受损胆管并恢复其功能,使得这些器官得以被移植给患者。这为肝脏治疗带来了新的选择,也为修复捐赠器官带来了新的可行思路。
《自然·生物医学工程》上一篇文章报道了复旦大学的邵志成团队开发了将星形胶质细胞诱导成为神经类器官的方法(Op53-CSBRY),形成的具有脊髓背侧和腹侧神经元功能的脊髓类器官移植给小鼠后,类器官可存活并分化为脊髓神经元,并与宿主神经元形成突触,改善小鼠的运动功能。
总结
类器官已经在多项研究中被证明具有较强的移植修复能力,且安全性良好。其在肠道、肝脏、心脏等领域的研究较多,不过由于类器官非常复杂,对培养体系、血管系统、工程化等都有着较高的要求,当下大多尚处于早期研究阶段,要想实现临床转化仍还有很长一段路要走。未来随着类器官技术的发展,或许器官移植/再生医学领域将会迎来重大进展。