
近日,在Biomaterials发表了一篇名为”Two-dimensionally cultured functional hepatocytes generated from human induced pluripotent stem cell-derived hepatic organoids for pharmaceutical research“的研究论文,由大阪大学药学研究科的水口裕之教授领导的研究团队完成。该研究利用人诱导多能干细胞(iPSC)来源的肝类器官(iHOs),通过优化培养条件和开发二维(2D)培养方案,成功获得了功能强大的iHO-Heps肝细胞。

01 研究背景
人诱导多能干细胞(iPSC)来源的肝细胞类细胞(HLCs)被认为是替代原代人肝细胞(PHHs)的潜在选择,用于药物研发。然而,HLCs存在一些局限性,如肝功能较低、分化时间长,且在终末分化后无法增殖,难以大量制备。为了克服这些问题,研究团队建立了iPS细胞来源的肝类器官(iHOs),并进一步开发了二维培养方案。
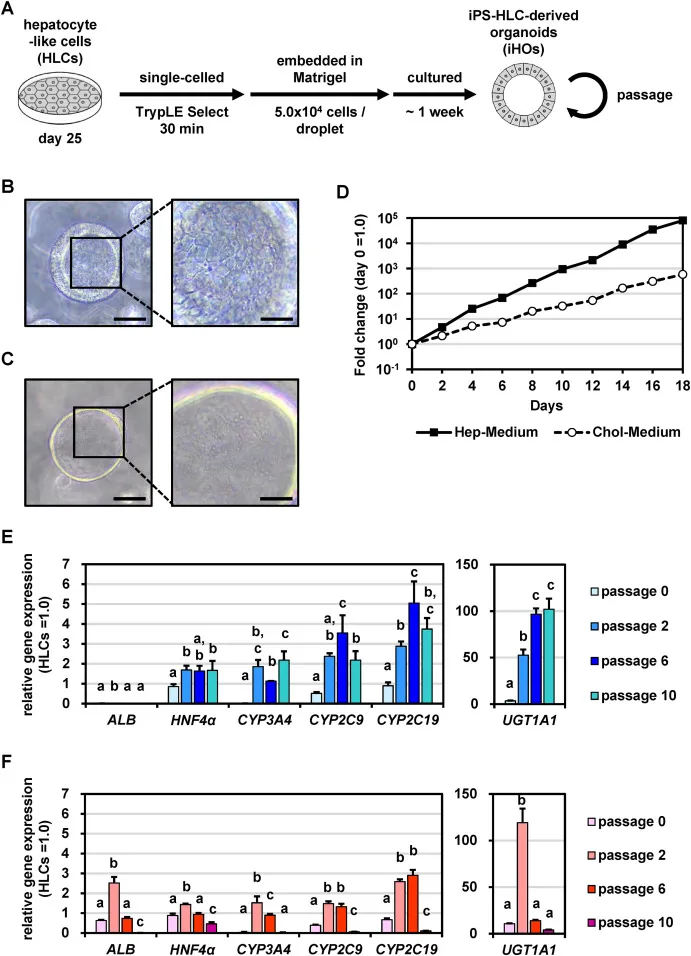
适合肝脏类器官建立和培养的培养基
02 研究结果
iHOs的增殖能力极高
研究团队通过优化培养基成分和培养条件,使iHOs能够在18天内增殖约10⁵倍,这一增殖速度比传统培养基快100倍。此外,iHOs在经过多次传代后(超过3次传代)仍能保持强大的增殖能力,甚至可以维持到第10代以上。这种高效的增殖能力为大规模制备功能性肝细胞提供了可能,也为后续的药物研发和毒性测试奠定了基础。
此外,研究还发现,从终末分化(第25天)的肝细胞样细胞(HLCs)建立的iHOs,更适合生成具有更高肝功能的肝细胞。这些结果表明,iHOs不仅具有强大的增殖能力,还能在传代过程中保持良好的细胞功能,为药物研发提供了理想的体外模型。
在基因表达水平上表现出显著的优势
RNA-seq分析显示,iHO-Heps在大多数主要肝细胞标记基因的表达水平上显著高于传统的肝细胞样细胞(HLCs)和未进行二维培养的iHOs,甚至在某些关键基因的表达上超过了原代人肝细胞(PHHs)。例如,iHO-Heps在药物代谢相关基因的表达上表现出更高的活性,特别是CYP3A4和CYP2C19的活性,甚至比PHHs更高。这表明iHO-Heps在药物代谢和毒性测试方面具有更接近人体生理状态的特性。
此外,二维培养条件使细胞从增殖状态转变为代谢状态,激活了药物代谢等相关通路,进一步增强了iHO-Heps的功能。这种基因表达水平的提升,使得iHO-Heps在药物研发中具有更广泛的应用潜力,能够更准确地模拟人体肝脏的代谢和毒性反应。
表现出多种典型的肝细胞功能
iHO-Heps展现出多种关键的肝细胞功能,包括糖原储存、摄取和释放吲哚菁绿(ICG)、分泌白蛋白和尿素以及形成胆小管的能力。这些功能不仅体现了iHO-Heps在代谢、解毒、蛋白质合成和胆汁运输等方面的活性,还表明其在二维培养条件下能够高度模拟真实肝脏的生理特性,使其成为药物研发和毒性测试中极具潜力的体外模型。
在药物代谢和毒性反应方面表现出显著的优势
iHO-Heps的多种细胞色素P450 (CYP)酶活性显著高于传统的肝细胞样细胞(HLCs),其中CYP3A4和CYP2C19的活性甚至超过了原代人肝细胞(PHHs)。在肝毒性药物的响应实验中,iHO-Heps对不同药物的敏感性与PHHs相似,表明其能够准确模拟药物在人体肝脏中的代谢和毒性反应。
总体而言,这项研究成功克服了传统的肝细胞样细胞(HLCs)的局限性,建立了优化的iPS细胞来源的肝类器官(iHOs)培养方案,通过2D培养获得的iHO-Heps具备多种关键肝功能和强大的药物代谢能力。这一成果为药物研发提供了更可靠的肝细胞模型,有助于更准确地评估药物代谢和毒性。同时,也为研究肝脏疾病发病机制和个性化药物治疗提供了新的工具。尽管目前仍有进一步优化的空间,但该研究无疑为医药研发领域带来了重要突破,有望推动未来医药研究的快速发展。