
香港大学李嘉诚医学院生物医学学院(以下简称“港大医学院”)的研究团队,近日在干细胞研究领域取得突破性进展,该团队研发出一种将血液及皮肤细胞转化为神经干细胞的创新方法。该研究成果的出现,一方面,克服了当前干细胞研究技术的局限性;另一方面,为治疗与年龄相关疾病(如帕金森病、阿尔茨海默病、肌萎缩侧索硬化症等),提供了新的选择与希望,相关研究结果同步发表在世界知名期刊《科学进步(Science Advances)》杂志中。
港大医学院:探索神经干细胞的研发捷径,治疗与年龄相关的疾病

▲截图源自“Science Advances”
人体由200余种不同类型的细胞组成,每种细胞在维持整体健康方面都发挥着关键作用。然而,获取和分析某些特殊类型的细胞(如位于大脑深处的神经元)一直较为困难。加之,传统的诱导多能干细胞(IPS)、胚胎干细胞通常无法完全捕捉衰老细胞的特征,限制了它们在治疗与年龄相关疾病方面的应用。
为了应对这些限制,港大医学院团队通过将一种名为“SOX17”的强大分子,转化为“超级干细胞因子”,使其在细胞核内自我组织,并精确地从一个基因导航到另一个基因,从而实现快速且有效的细胞转化。目前该团队已经提交了关于使用工程化SOX17的非临时专利申请,用于开发下一代干细胞模型,且保留了衰老干细胞,为研究与年龄相关疾病的潜在治疗方法,提供了更具参考价值的数据,下一阶段将针对老年人血液细胞中,产生的神经细胞进行研究。
“这些研究标志着干细胞研究领域的一个重要里程碑。我们可利用干细胞,治疗与衰老相关的多种疾病,解锁个性化的治疗策略,以满足个别患者的独特需求!”——港大医学院副教授兼转化干细胞生物学中心首席研究员Ralf Jauch教授
衰老小科普
衰老是指随着年龄的增长,身体逐渐退化,表现为衰老细胞和炎症因子的积累,从而导致各种衰老相关疾病的发生,比如神经退行性疾病、骨质疏松症、卵巢早衰(POF)、心血管疾病(CVD)等。
衰老通常伴随着细胞衰老,这是衰老的关键机制。此外,内源性干细胞耗竭也可能参与了衰老的过程。与年轻的间充质干细胞(MSC)相比,衰老的间充质干细胞(MSC)会出现细胞活性下降、免疫调节能力下降、分泌因子(如抗炎因子、生长因子等)的能力下降。此外,衰老细胞的形态也会有所变化,比如随着脐带间充质干细胞(hUC-MSCs)的衰老,细胞形态可从细长的梭形,变为大而扁平的的形状(详见下图)。
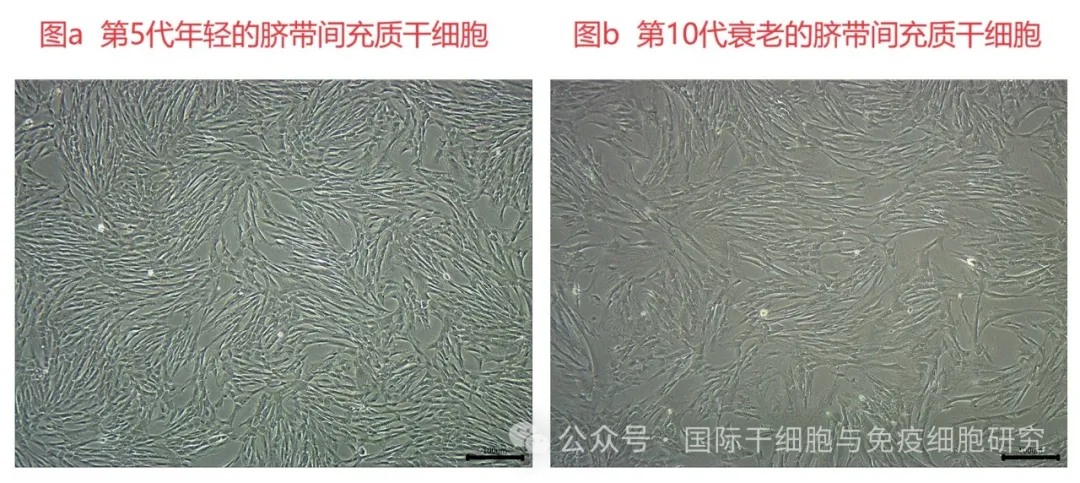
▲图源“PMC”
如何延缓衰老?
目前研究发现,以间充质干细胞为代表的细胞疗法,是延缓及对抗衰老相关疾病的潜在治疗方法。此外,适当的营养干预、加强运动、热量限制、维持铁稳态等方法,也在一定程度上有助于延缓衰老的进程。
细胞疗法对抗皮肤衰老
皮肤作为机体的屏障,会随着衰老而发生老化或病理改变,皮肤状态也是衰老的直观表现之一,可能是由衰老细胞的积累、胶原蛋白的丢失、基质金属蛋白酶及氧化活性的增加所致。
研究显示,间充质干细胞(MSC)是一种多能细胞,可在体内和体外产生间充质和非间充质组织,并具有自我更新、多向分化能力。MSC可分泌皮肤再生所需的因子、抑制基质金属蛋白酶的表达、增加胶原蛋白的合成,在皮肤再生中具有良好的应用前景。
此外,紫外线也是造成皮肤衰老的关键因素之一,易损伤皮肤真皮层、破坏纤维组织,由此引发的衰老问题又被称为“光老化”。间充质干细胞可通过增加细胞增殖、新血管形成,来促进皮肤的再生。此外,还可通过组织结构再生、产生胶原蛋白和弹性蛋白纤维等,预防紫外线引起的衰老问题。
细胞疗法对抗衰老引起的毛发问题
脱发、白发也是衰老的直接表现之一。其中,脱发与毛囊退化有关,虽然目前可通过手术(如植发术)或药物(如米诺地尔)进行治疗,但其疗效有限,并不适合所有患者,且存在一定的副作用。因而,急需研发更加有效的治疗脱发的方法。
研究显示,间充质干细胞(MSC)具有迁移、归巢和分化的能力,且具有旁分泌作用,可释放多种营养因子(如细胞因子、生长因子等),在毛发再生和修复中,起着重要的作用,可用于脱发治疗的常见干细胞如下:
1、骨髓间充质干细胞(BMSC):可促进毛囊干细胞(HFSC)增殖,使毛囊从静止期,转变为生长期,从而促进毛囊再生及毛发生长。
2、脐带间充质干细胞(hUC-MSC):具有保护毛囊真皮乳头细胞,并治疗脱发的能力。
3、其他干细胞细胞:如毛囊间充质干细胞、牙髓间充质干细胞、脂肪间充质干细胞、羊水间充质干细胞等,也能加速毛发再生,对脱发有一定的治疗作用。
细胞疗法对抗免疫衰老
衰老会导致免疫系统衰老,破坏巨噬细胞的稳态,增加老年人的发病率和死亡率,这种现象被称为免疫衰老。随着老年人寿命的迅速增加,免疫系统逐渐成为与年龄相关的疾病的主要驱动因素。免疫系统衰老是一种动态、渐进的过程。研究显示,人体在30岁以后,胸腺活性会以每年2%~3%的速度逐年下降,从而导致50~65岁个体的活性显著降低,虽然衰老的胸腺仍会继续发挥免疫功能,但T细胞产量显著减少,其效果可能也会大打折扣。比如神经退行性疾病、心血管疾病、骨质疏松症等,都是与衰老相关的常见疾病。
因而,如何重建或提升机体免疫力,是对抗与衰老相关疾病的重要手段之一。近年研究发现,细胞疗法有助于抵消免疫衰老和与年龄相关的免疫功能障碍,介入性免疫再生策略主要存在两种思路,其一,侧重于再生衰老的免疫器官,以重启患者的免疫系统;其二,通过人工补充细胞、微环境或组织,直接重建免疫系统。下面以临床常用的干细胞和NK细胞为例,简单介绍一下如何通过细胞疗法,提高机体免疫力。
1、间充质干细胞(MSC)
间充质干细胞(MSC)具有独特的免疫调节能力,参与组织再生、维持体内平衡。
一方面,可直接影响先天性和适应性免疫细胞(如NK细胞、DC细胞、巨噬细胞、B淋巴细胞、T淋巴细胞),以恢复免疫稳态。
另一方面,间充质干细胞是胸腺退化的已知调节剂,可调节胸腺的结构和活动,预防、减缓或逆转胸腺退化的过程。
2、NK细胞
自然杀伤细胞(natural killer,NK)是天然免疫的核心细胞,时刻在全身血管内巡逻,行使着免疫监视功能,会在第一时间发现并清除癌细胞、感染细胞、衰老细胞等“异己”,故又被誉为机体抗癌、抗感染的第一道防线,在清除肿瘤、对抗感染方面发挥关键作用。
NK细胞还可作为适应性免疫的关键调节剂,因其可通过靶向树突状细胞,调节适应性免疫;还可通过释放趋化因子、炎性细胞因子、细胞溶解颗粒等,来激活和募集先天和适应性免疫反应的成分。
细胞疗法改善卵巢早衰(POF)
卵巢早衰(POF)是一种常见的内分泌疾病,可导致女性不孕,其发病可能与自身免疫、基因缺陷、化疗损伤、年龄等多种因素有关。随着年龄的增长,大部分卵泡耗竭,卵巢功能受损,最终可导致卵巢早衰。目前以激素治疗为主,但该方法无法恢复卵巢功能。
干细胞疗法的出现为卵巢早衰患者带来了新的希望。研究显示,间充质干细胞具有免疫调节作用,可增加抗炎因子的释放、抑制促炎因子的产生,从而有助于促进卵泡存活、改善卵巢早衰。
一项关于“脐带间充质干细胞(UC-MSC),治疗卵巢早衰”的研究,将入组患者分为两组,即干细胞治疗组(接受UC-MSC移植)、联合治疗组(接受UC-MSC联合胶原移植)。经过为期1年的随访,结果显示,间充质干细胞在治疗卵巢早衰方面具有良好的效果。其中,UC-MSC改善了卵泡的激活和生长;而UC-MSC联合胶原移植,则有助于卵巢功能的长期恢复,并在一定程度上提高了患者的生育能力。
细胞疗法改善神经退行性疾病
随着衰老的进展,一些神经退行性疾病(如阿尔兹海默病、帕金森病等)的发病率也随之增加,衰老是神经退行性疾病的主要危险因素之一。
研究显示,间充质干细胞(MSC)具有迁移和归巢能力,在衰老的大脑中发挥作用;此外,神经干细胞(NSC)可产生新的神经元,有助于改善中枢神经系统的功能。
细胞疗法改善骨质疏松
骨质疏松症是一种与年龄有关的进行性全身性骨病,其特征是骨量低、骨脆性大。在骨质疏松症患者中,MSC分化为成骨细胞的能力降低,但分化为脂肪细胞的能力增强,最终导致骨形成减少。虽然部分药物有助于治疗本病,但并非对所有患者有效,而且还可能产生不良反应。因此,迫切需要新型治疗方法。
近年研究显示,间充质干细胞(MSC)不仅能分泌参与骨修复的因子,还具有分化为成骨细胞、软骨细胞、脂肪细胞的能力。因此,MSC可作为与年龄相关的骨质疏松症的替代疗法,在骨质疏松的治疗中,具有广泛的应用前景。
▼间充质干细胞治疗衰老相关疾病的临床研究
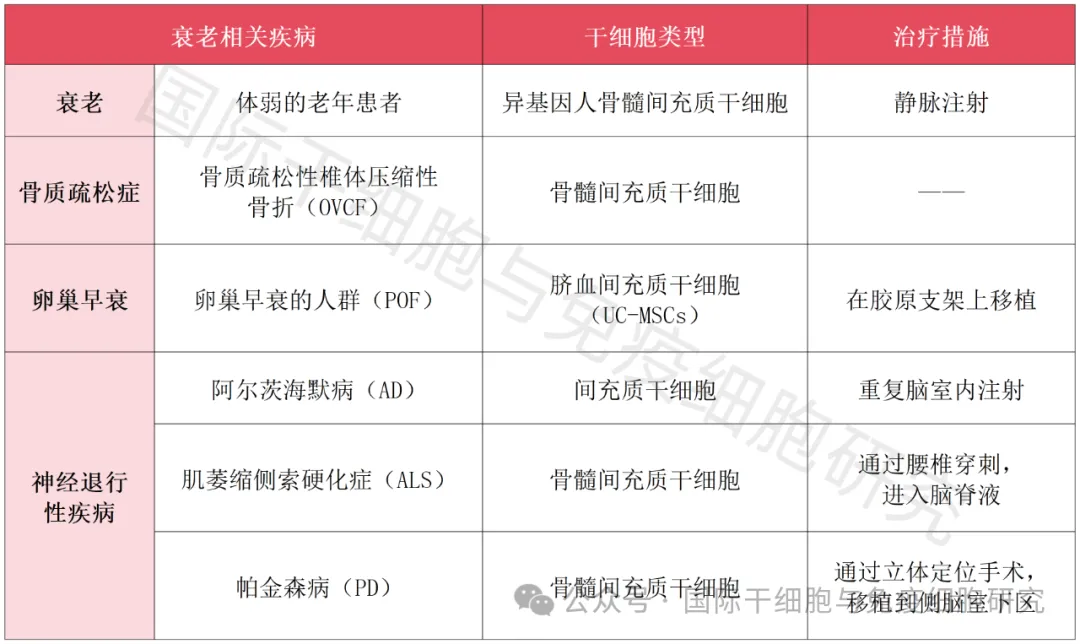
▲数据源自“Stem Cell Res Ther”,国际干细胞与免疫细胞研究医学部整理汇总
小编寄语
衰老不仅影响我们的外观,还可能会引起多种年龄相关疾病,比如脱发、神经退行性疾病、骨质疏松症、卵巢早衰等,对人体的危害较大。因而,深入了解衰老的原因,探索更有效的措施,来延缓甚至逆转衰老,具有的重要意义。
近年研究发现,随着再生医学的发展,以干细胞为代表的细胞疗法,在抗衰老领域具有广阔的应用前景,有助于延缓衰老、对抗与衰老相关的疾病、提升机体免疫力。值得欣慰的是,目前已有一些基于干细胞治疗衰老及衰老相关疾病的临床试验,初步证明了细胞疗法的有效性和安全性。
参考资料
[1]Wang Y,et al.Application of mesenchymal stem cells for anti-senescence and clinical challenges. Stem Cell Res Ther. 2023 Sep 19;14(1):260.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10510299/
[2]Weng M,et al.An engineered Sox17 induces somatic to neural stem cell fate transitions independently from pluripotency reprogramming[J].Science advances,2023,9(34):eadh2501.
https://www.science.org/doi/full/10.1126/sciadv.adh2501?rfr_dat=cr_pub++0pubmed&url_ver=Z39.88-