
再生医学浪潮翻涌,多能干细胞疗法凭借其巨大的应用潜力与不断涌现的突破性成果,正跃升为全球医疗领域最炙手可热的赛道。
近来,这一前沿领域传来振奋人心的进展 —— 不仅为难治性疾病的治疗开辟了全新路径,更给整个再生医学的发展注入了强劲动能,让攻克疑难病症的希望愈发清晰。
Cell重磅:人类胚胎干细胞来源的多巴胺能前体细胞,安全有效治疗帕金森病
2025年10月13日,高丽大学附属安岩医院、延世大学医学院、成均馆大学医学院及S. Biomedics公司的研究人员合作,在国际顶尖学术期刊Cell上发表了题为:Phase 1/2a clinical trial of hESC-derived dopamine progenitors in Parkinson’s disease的研究论文。
该研究开发了人类胚胎干细胞(hESC)来源的多巴胺能前体细胞(A9-DPC),在1/2a期临床试验中,双侧壳核移植A9-DPC表现出良好的安全性,并能有效改善帕金森病患者的运动症状,且具有剂量依赖性疗效特征。
鉴于帕金森病明确的病理特征——特定多巴胺能神经元群的丧失,帕金森病长期以来一直被视为细胞再生疗法的理想候选对象。尽管多巴胺能细胞移植目前被认为是一种部分多巴胺补偿的对症治疗方法,但它与传统疗法不同,能够补充丧失的多巴胺能神经元,并在纹状体区域实现持续、空间定位的多巴胺释放。因此,研究人员致力于通过向壳核移植多巴胺能细胞来实现多巴胺功能的定向恢复。
基于之前的临床前研究,韩国食品药品安全部(MFDS)批准了将人类胚胎干细胞(hESC)来源的多巴胺能前体细胞(A9-DPC,TED-A9)移植到帕金森病患者大脑中。
技术路线
在这篇最新论文中,研究团队报告了评估A9-DPC移植在帕金森病患者中的安全性和探索性疗效的1/2a期临床试验的1年中期结果。
在这项单中心、开放标签、剂量递增的1/2a期临床试验中,12名重度帕金森病患者在免疫抑制方案下进行了双侧壳核移植治疗,低剂量组的6名患者移植了315万个细胞,高剂量组的6名患者移植了630万个细胞。
结果显示:安全性优异,未观察到剂量限制性毒性或移植相关不良事件。患者运动功能得到改善,移植12个月后,在停药状态下,MDS-UPDRS第三部分评分显著改善,Hoehn-Yahr分期得到优化,高剂量组运动功能改善幅度更大。多巴胺转运体正电子发射断层扫描(PET)成像显示,双侧后壳核多巴胺摄取量增加,高剂量组摄取提升更显著,证实了移植细胞的存活。
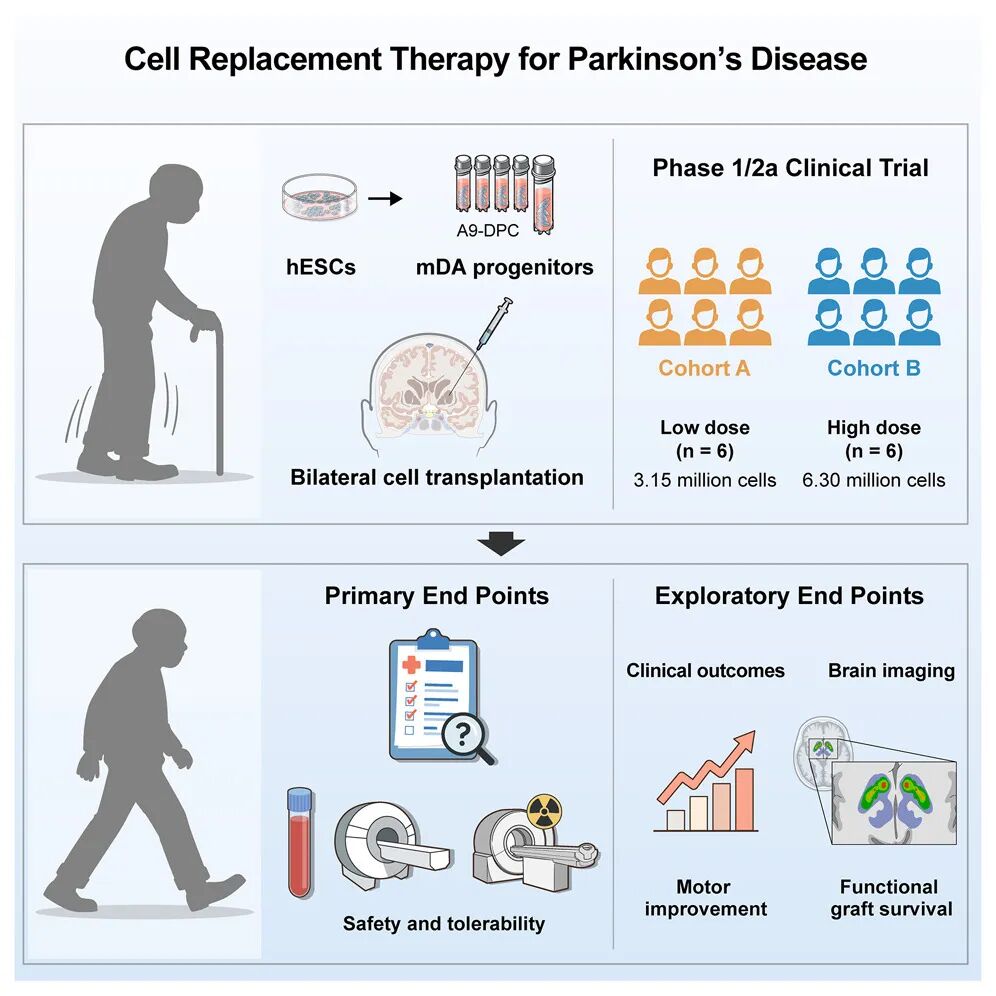
图形摘要
该研究的亮点:
1. 从人类胚胎干细胞(hESC)中生成了高纯度的多巴胺能前体细胞(A9-DPC);
2. 在帕金森病患者中,双侧核壳移植A9-DPC是安全的;
3. A9-DPC移植改善了帕金森病患者的运动症状,高剂量时效果更显著;
4. 正电子发射断层扫描(PET)显示多巴胺转运体结合增加,尤其是在高剂量组中。
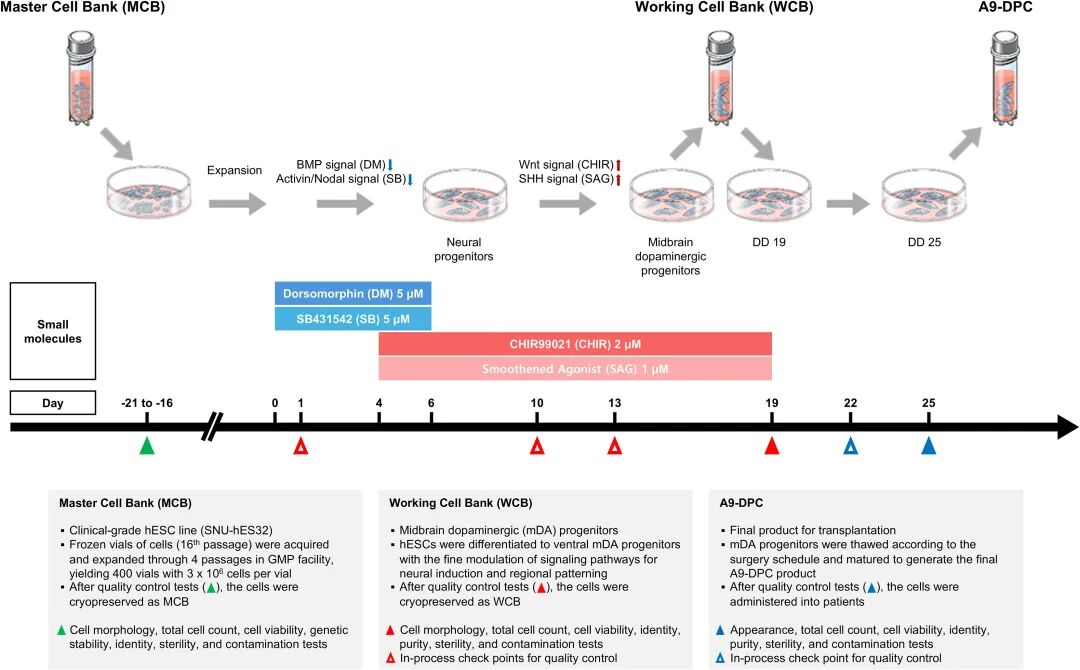
A9-DPC制备示意图
Cell 子刊:中国科学家突破帕金森细胞治疗瓶颈
近日,中国科学院脑科学与智能技术卓越创新中心陈跃军团队和复旦大学熊曼团队合作,在Cell Stem Cell上发表了题为:3D-generation of high-purity midbrain dopaminergic progenitors and lineage-guided refinement of grafts supports Parkinson’s disease cell therapy 的研究论文。
该研究开发了一种3D培养技术,能够高效、稳健地生成高浓度中脑多巴胺祖细胞(mDAPs),还可以结合单细胞空间转录组学和谱系追踪技术,洞察移植细胞的分化分布,为推动更安全、高效的帕金森病细胞替代疗法奠定了基础。

技术路线
研究团队创新开发了一套细胞制备与评估策略:
在细胞生成层面,团队基于双报告基因hESC细胞系,通过精确调控WNT和SHH信号通路,建立了全流程3D、无外源因子的分化体系(SphereDiff)。SphereDiff方法模拟体内中脑发育微环境,可以实现高效生成mDAPs及mDA神经元。该系统在多种hESC和hiPSC系中均表现出高度可重复性,克服了批次间稳定性问题。
为解决「盲盒移植」难题,团队开发了交叉移植单细胞分裂条形码(TX-SISBAR)技术,首次在单克隆水平绘制了移植细胞的谱系命运。利用这一技术,他们发现了mDAPs主要分化为DA神经元和星形胶质细胞,而间脑祖细胞则会产生无关的谷氨酸能神经元。这一结果不仅阐明了移植供体的细胞谱系多样性,也为下一步靶向消除非目标细胞、提升安全性提供了理论依据。
基于此,团队进一步优化了 SphereDiff 分化工艺,通过分阶段调控WNT信号以减少非靶向细胞群的产生。实验证实,调整后的体系实现了更高纯度的DA神经元移植。
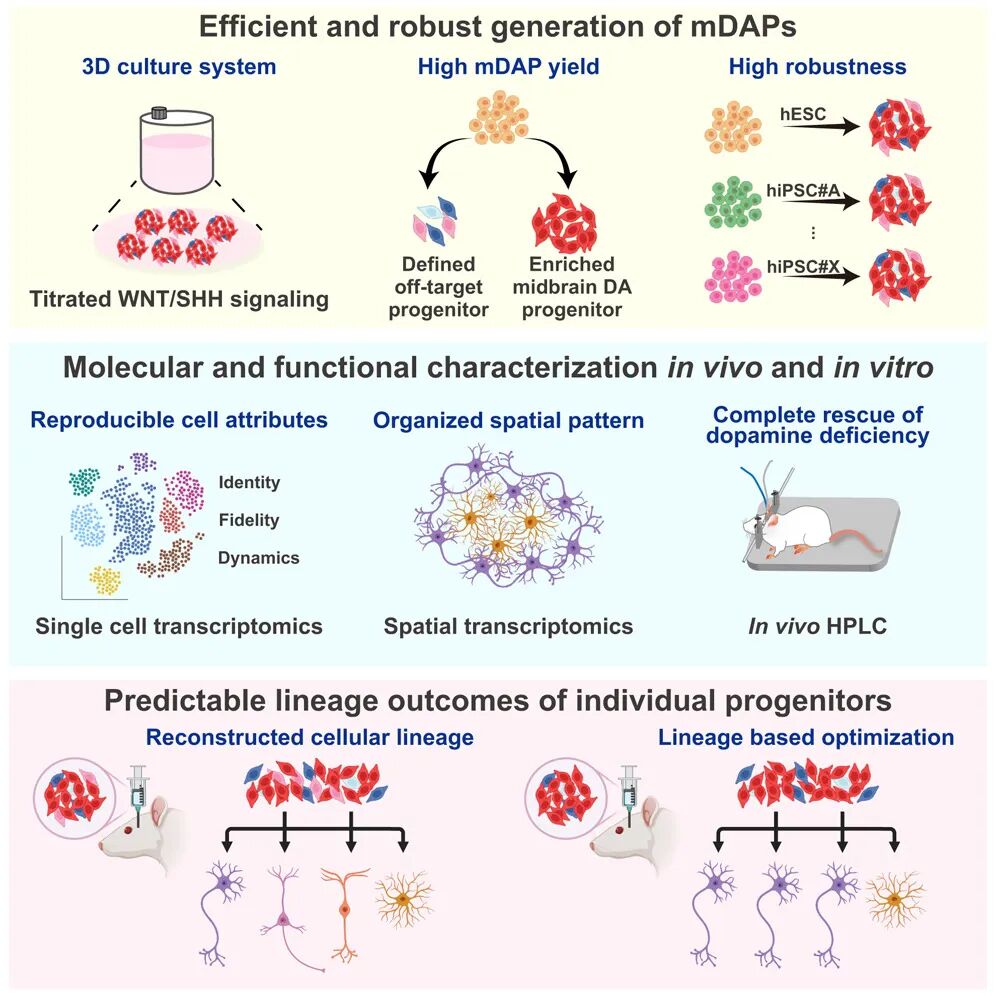
图形摘要
动物实验和单细胞组学分析显示,该体系制备的供体细胞不仅能在体内高效生成功能成熟的DA神经元,显著恢复PD模型动物的运动与多巴胺代谢功能,还可实现不同谱系的高分辨率追踪和空间定位,明确移植物细胞组成及分化来源。
总的来说,这项研究开发的SphereDiff方法,是PD细胞替代疗法领域的重大突破,其谱系引导的分化优化还可以有效消除非靶向细胞,为临床移植安全性提供了理论和技术支撑。
总结
这两项研究从不同维度推动了帕金森病细胞替代疗法的发展:韩国研究聚焦临床转化,验证了细胞移植的临床价值;中国研究侧重技术创新,解决了细胞制备与移植安全性的关键问题。二者共同为再生医学在帕金森病治疗领域的应用奠定了更坚实的基础,也让全球范围内通过干细胞疗法攻克疑难病症的目标更进一步,为广大患者带来了新的希望。